Menu
Medical Device Regulation (MDR) - Rozporządzenie w sprawie wyrobów medycznych
Gotowy na nowe Rozporządzenie MDR z Amoena
Rozporządzenie w sprawie wyrobów medycznych (MDR) to europejskie rozporządzenie dotyczące wyrobów medycznych, które weszło w życie z końcem maja 2017 r. (UE 2017/745). Po okresie przejściowym, przedłużonym z powodu pandemii koronawirusa, nowe wymagania zaczynają obowiązywać od 26 maja 2021 roku. Wymaga to wprowadzenia istotnych zmian dla producentów wyrobów medycznych, jak i dystrybutorów, nie później niż do tej daty.
Amoena jest dobrze przygotowana do stosowania nowego rozporządzenia w sprawie wyrobów medycznych. Wdrażając wymagania MDR, uczyniliśmy je jak najbardziej praktycznymi, prostymi i przejrzystymi dla obu stron - dla nas jako producenta i dla naszych partnerów dystrybucyjnych.
Jakie są widoczne efekty MDR?
Zgodnie z MDR na etykietach wyrobów medycznych wymagane są rozszerzone informacje. Oprócz kodu, który jednoznacznie identyfikuje produkty, na opakowaniu i etykiecie znajdą Państwo dalsze dane i symbole. Produkty, za które odpowiada Amoena Medizin-Orthopädie-Technik GmbH (producent i dystrybutor) można zidentyfikować na podstawie adresu umieszczonego tuż za czarnym symbolem fabrycznym na etykiecie lub opakowaniu:
 Amoena Medizin-Orthopädie-Technik GmbH
Amoena Medizin-Orthopädie-Technik GmbH
Kapellenweg 36, 83064 Raubling, Germany
www.amoena.com
Co dzieje się ze starszymi produktami (patrz art. 120 ust. 4 MDR)?
Produkty z dotychczasowymi etykietami mogą być sprzedawane przez sklepy specjalistyczne do maja 2025 r., o ile termin ważności produktów nie zostanie wcześniej przekroczony.
Dotyczy to również produktów, które dotarły do sklepu medycznego przed 26 maja 2021 r. Uważa się, że zostały one już wprowadzone do obrotu i nie wymagają ponownego oznakowania.
Jakie są nowe wymagania dotyczące etykietowania produktów?
Oprócz znanego znaku CE, znajdziecie Państwo również kilka nowych symboli, które przedstawiamy poniżej:
Ikona | Wyjaśnienie |
 | Termin ważności: Wraz z wejściem w życie rozporządzenia MDR produkty muszą być oznakowane datą produkcji lub datę ważności wyrobu. Nasze protezy piersi i produkty do pielęgnacji protez piersi są oznaczane datą ważności. Termin ważności określa się na podstawie badań dotyczących okresu trwałości. Przeterminowane produkty nie mogą być już sprzedawane. |
 | Data produkcji Wraz z wejściem w życie rozporządzenia MDR produkty muszą być oznakowane datą produkcji lub datę ważności wyrobu. Nasze produkty opieki pooperacyjnej Recovery Care i inne wyroby tekstylne są opatrzone datą produkcji. |
 | Numer katalogowy: Symbol ten jest umieszczony przed każdym numerem artykułu. |
 | Seria i numer: Symbol ten jest umieszczony przed numerem seryjnym wyrobu. |
 | Numer partii produkcyjnej: Symbol ten jest umieszczony przed numerem partii produkcyjnej. |
 | Symbol „MD” oznacza wyroby medyczne – umieszcza się go, aby wskazać, że produkt stanowi wyrób medyczny. |
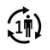 | Jeden pacjent - wielokrotne użycie: Produkt może być używany wielokrotnie tylko przez jednego pacjenta. |
 | Więcej informacji w instrukcji użycia. |
| | W przypadku uszkodzenia opakowania, produkt nie powinien być użytkowany. |
 | „Czarna” fabryka symbolizuje producenta. Można go znaleźć na pudełku kartonowym lub etykiecie na opakowaniu. Obok symbolu zawsze umieszcza się adres firmy Amoena GmbH. |
 | Ochrona przed światłem słonecznym. |
 | Przechowywanie w suchym miejscu. |
Obowiązek raportowania incydentów.
W mało prawdopodobnym przypadku „poważnego incydentu” z wyrobem medycznym należącym do naszej klasy ryzyka, ustawodawca zobowiązuje nas do raportowania, zgodnie z informacją zawartą w instrukcji użytkowania wyrobu. Ponadto, zgodnie z wymogami MDR, nasze aktualne instrukcje użytkowania można znaleźć na naszej stronie internetowej.
W przypadku dalszych pytań dotyczących MDR prosimy o kontakt: mdr-pl@amoena.com
.





